چرا ما بیش از والدین مان دارو می خوریم؟
شاید شما هم گاهی که قرص می خورید از خودتان بپرسید چرا این همه دارو می خورم؟
شاید مادرتان از دیدن کیف داروهایتان غصه می خورد. یا از پزشکتان بخواهید که بیش از این برایتان دارو تجویز نکند.
آیا انسان های عصر جاری ، از گذشتگان خود بیمارتر ، ضعیف تر، یا در برابر بیماریها آسیب پذیرتر هستند؟
-بسیاری از موارد وقتی برای بیمار دارو تجویز می شود ، علیرغم اینکه برای کمک به حل مشکلش مراجعه کرده است، با مصرف دارو مخالفت می کند و می گوید “ من همین حالا هم تعداد زیادی قرص مصرف می کنم. نمی خواهم اینقدر دارو بخورم”
-یکی از باورهایی که در زمینه ی اینگونه مقاومت ها وجود دارد این است که “ما از نسل های قدیمی بیشتر دارو می خوریم ، چون ضعیف تر یا بیمارتر هستیم” که باور نادرستی است.
-در واقع دلیل اینکه بیشتر دارو می خوریم پیشرفت علم ، از جمله علم پزشکی، است. پیشرفت علوم ، از یک طرف، باعث شده است که قدرت تشخیص پزشکان بالاتر برود. یعنی ما می توانیم بیماری ها و اختلالات را با جزئیات بیشتر و در مراحل زودتر شناسایی کنیم.
-بنابراین ، امروزه بیماری هایی را تشخیص می دهیم که نسل های قبل ابزار کافی برای شناسایی آنها نداشتند و وقتی اختلال پیشرفت می کرد و علائم شدیدتری ایجاد می نمود، برای درمان آن اقدام می کردند.
-از سوی دیگر، پیشرفت علوم باعث شده که داروهای تخصصی تر ومتنوع تری در دسترس مان باشد. یعنی امروزه ، نسبت به قبل، حتی برای اختلالات کوچک نیز داروهایی تخصصی و منحصر به فرد داریم. -پس هم بیشتر بیماری ها را شناسایی می کنیم ، و هم برای درمان آنها ابزارهای متنوع تر و تخصصی تری داریم
-درست مثل یک نجار امروزی که نسبت به نسل های گذشته، ابزار و آلات متنوعتر و ظریف تری در اختیار دارد و محصولات بهتری هم تولید می کند. یا وسایل آشپزخانه ی این نسل که چندین برابر نسل های گذشته هستند.
-پس، اینکه شما بیشتر از والدین تان دارو می خورید، اتفاقی مثبت است .
- منتشر شده در داروها
لورازیدون موافقت FDA را برای افسردگی دوقطبی در کودکان دریافت کرد
سازمان غذا و داروی آمریکا ( FDA) کاربرد جدید لورازیدون را برای درمان اپیزودهای افسردگی ماژور همراه با اختلال دوقطبی ۱ ( افسردگی بای پولار) در کودکان و نوجوانان ۱۰ تا ۱۷ ساله تایید کرد.
لورازیدون، یک آنتاگونیست دوپامین سروتونین است که در حال حاضر در ایالات متحده به صورت منوتراپی یا درمان تکمیلی با لیتیم یا والپروات، برای درمان اسکیزوفرنی در بالغین و نوجوانان ۱۳ تا ۱۷ ساله تایید شده است.
ایمنی و اثربخشی این دارو برای افسردگی دوقطبی در کودکان ۱۰ تا ۱۷ ساله، در یک مطالعهی شش هفتهای، تصادفی، دوسوکور، با کنترل پلاسبو ارزیابی شده است. ۳۴۷ شرکت کننده، تکدوز روزانهی لورازیدون ( 20-80 mg/day ) یا پلاسبو دریافت کردند.
لورازیدون در مقایسه با پلاسبو، بهبودی بالینی معنادار در علائم افسردگی دوقطبی نشان داد. نشانهی اولیهی اثر بخشی، تغییر نمرهی مقیاس افسردگی کودکان در هفتهی ششم نسبت به نمرهی پایه بود ( p<.0001).
این دارو عموما خوب تحمل شد. شایعترین عوارض ناخواستهی درمان تهوع، افزایش وزن، و بیخوابی بود.
این، اولین فرمولاسیون تک-دارویی است که برای این اندیکاسیون در کودکان پذیرفته شده است.
لورازیدون به صورت قرصهای ۲۰، ۴۰، ۸۰ و ۱۲۰ میلیگرم در دسترس است.
شرکت سازنده اشاره میکند که استفادهی طولانیتر ( بیش از ۶ هفته) هنوز در مطالعات کنترل شده بررسی نشده است و به پزشکان توصیه میکند در صورت انتخاب این دارو برای درمان طولانیتر، اثربخشی دارو برای هر بیمار را مجددا ارزیابی نمایند. تاثیر لورازیدون در درمان مانیا هنوز اثبات نشده است.
منبع : Medscape.com
- منتشر شده در بیماری ها, داروها, کودک و نوجوان
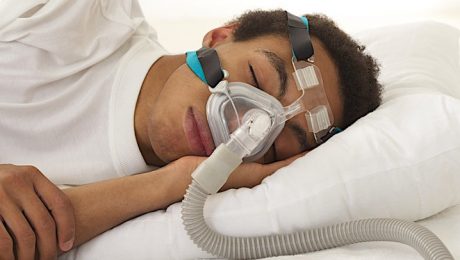
اثرات درونابینول در آپنه انسدادی خواب
در حال حاضر درمان دارویی تایید شدهای برای آپنه خواب وجود ندارد و درمان انتخابی، استفاده از CPAP است که از فشار دائمی هوا برای باز نگه داشتن مجاری هوایی استفاده میکند. با وجود اثربخشی، استفاده از این وسیله پر زحمت است و کمتر به صورت مداوم استفاده میشود.
درونابینول، فورمولاسیون صناعی اختصاصی مولکول دلتا-۹ THC
و آگونیست غیر اختصاصی رسپتورهای نوع ۱ و ۲ کانابینوئیدی ست که توسط FDA در ابتدا برای تهوع و استفراغ همراه با کموتراپی تایید شد و برای تقویت اشتها در سندرم کاهش وزن ناشی از ایدز نیز اندیکاسیون دارد.
در مطالعهای که در ژانویه ۲۰۱۸ در مجلهی Sleep منتشر شده، اثرات این دارو بر آپنه انسدادی خواب ، در فاز ۲ مطالعهی *PACE بر روی ٧٣ بیمار بزرگسال با آپنهی خواب متوسط یا شدید بررسی شد.
بیماران به صورت تصادفی در سه گروه تقسیم شده و ٢/٥ mg درونابینول، ١٠ mg درونابینول، و پلاسبو، یك ساعت قبل از خواب دریافت نمودند. متوسط BMI پایه ٣٣/٤ kg/m2 و متوسط سن، ٥٣/٦ سال بود. متوسط نمرهی AHI** ، ٢٥/٩ و متوسط نمرهی معیار خواب Epworth ، ١١/٥ بود.
هدف ابتدایی مطالعه، تغییر AHI از مقدار پایه بعد از شش هفته درمان در نظر گرفته شد.
مطالعه، بهبودی قابل توجه را در گروه ٢/٥ میلی گرم ( كاهش ١٠/٥ رخداد در ساعت p=0.02) و همچنین در گروه ١٠ میلی گرم ( كاهش ١٢/٩ رخداد در ساعت p=0.004)، در خواب REM و نیز NREM، و بعد از اصلاح عوامل سن، نژاد، قومیت، و AHI پایه، نشان داد. در گروه پلاسبو بعد از اصلاحات فوق، تغییر معناداری مشاهده نشد و تفاوت گروههای ٢/٥ و ١٠ میلیگرم نیز معنادار نبود.
همچنین، كاهش خواب آلودگی روزانه سابجكتیو در گروه ١٠ mg معنادار بود ( p<0.0001) در حالیكه در گروه ٢/٥mg و پلاسبو، معنادار نبود.
بیمارانی كه دوز ١٠ mg دریافت كردند بالاترین میزان رضایت از دارو را بر اساس پرسشنامهی رضایت از دارو گزارش كردند.
تغییراتی در معیارهای آبجكتیو تست MWT ، شامل تاخیر خواب، ساختار كلی خواب، مقیاسهای اكسیژناسیون طول شب، در هیچكدام از گروه ها مشاهده نشد.
در طول مطالعه ٧ بیمار به علت عوارض ناخواسته، و ١٠ بیمار به سایر علل، دارو را قطع كردند. تفاوت قابل توجهی در میزان ترك مطالعه بر اساس گروه بندی، BMI، پایه AHI، یا سایر عوامل وجود نداشت و میزان عوارض ناخواسته بین كسانی كه مطالعه را كامل كردند، و نكردند، مشابه بود. اگرچه اكثریت بیماران(٨٨٪) یك یا بیشتر عوارض جانبی را در طول مطالعه تجربه كردند، اكثر آنها خفیف بود و بین گروهها از نظر تعداد یا شدت عوارض تفاوت قابل توجهی وجود نداشت. یك عارضه جانبی جدی وجود داشت، اسهال و تهوع، كه بیمار برای هیدراتاسیون و پایش در بیمارستان بستری شد. بعد از ٢٤ ساعت ترخیص شد و مطالعه را تكمیل كرد. تغییر وزن بیماران در گروهها تفاوتی نداشت.
به عقیده نویسندگان مقاله بهبودی در هر دو خواب REM و NREM یافتهی قابل توجه مطالعه بود.
نهایتا، اگرچه این مطالعه پیشرفتی در درمان فارماكولوژیك آپنهی انسدادی خواب نشان میدهد، مطالعهی فاز ٢ بوده، و برای استفاده ی بالینی نیاز به تكرار مطالعات بزرگتر، فاز ٣، وجود دارد.
Pharmacotherapy for Apnea by Cannabimimetic Enhancement *
Apnea/Hypopnea Index **
وارنیكلین برای ترك سیگار با حوادث قلبی ارتباط دارد
American J of Respiratory and Critical Care Medicine , December 20, 2017
در كارآزماییهای بالینی تصادفی، #وارنیكلین در ترك سیگار موثرتر از #بوپروپیون، جایگزینهای #نیکوتین، روشهای غیر دارویی و پلاسبو بوده است. اما گزارشهای متعارضی درباره عوارض ناخواسته قلبی- عروقی و نوروسایکیتریک وجود دارد. به منظور بررسی این موارد، مطالعه مشاهدهای در کانادا به روی ۵۶۸۵۱ بیمار مصرف كننده این دارو انجام شد. محققین عواقب كاردیوواسكولار و نوروسایكیتریك را در طول ١٢ هفته تجویز دوز كامل این دارو، و در طول دوره كنترل ( شامل یك سال قبل از شروع وارنیكلین و یك سال بعد از آن به جز ١٢ هفته درمان و ٦ هفته اینداكشن دارو) مقایسه كردند.
نتایج قلبی- عروقی شامل MI حاد، آنژین ناپایدار، سایر اختلالات ایسكمیك قلبی، استروك ایسكمیك، نارسایی قلبی، دیسریتمیهای قلبی، و بیماری عروق محیطی كه منجر به ویزیت در اورژانس یا بستری در بیمارستان شده بود.
رخدادهای نوروسایكیتریك آسیب عمدی به خود، اپیزودهای افسردگی یا دوقطبی، اختلالات سایکوتیک، اضطراب، اختلالات نوروتیک، مرتبط با استرس، بیخوابی، توهم، و خشونت و بیقراری منجر به ویزیت اورژانس یا بستری در نظر گرفته شد.
نتایج: میزان بروز حوادث قلبی- عروقی به صورت معناداری در ۱۲ هفته درمان بیش از دوره کنترل بود.
برعکس، افزایش بروز عواقب نوروسایکیتریک در طول دوره درمان با وارنیکلین نسبت به دوره کنترل، معنادار نبود.
افراد مسنتر ( >۶۵ ساله) افزایش خطر قابل توجهی برای عواقب نوروسایکیتریک، عمدتا اختلالات اضطرابی و خلقی نیازمند ویزیت اورژانس یا بستری، در طول دوره ۱۲ هفته درمان نشان دادند. ( نسبت به سایر گروههای سنی)
نویسندگان مقاله تاکید میکنند که با توجه به مشاهدهای بودن مطالعه و سایر محدودیتها هنوز نمیتوان وارنیکلین را مسوول حوادث قلبی عروقی دانست. با توجه به اثرات بسیار مهم و اثبات شدهی قطع مصرف سیگار بر بیماریهای کاردیوواسکولر و سرطان و بالاتر بودن اثربخشی این دارو نسبت به سایر روشهای موجود، انتخاب وارنیکلین، منطقی است. اما لازم است پزشک بیمار را از کلیه یافتههای موجود آگاه سازد و در صورت تجویز این دارو، پایش دقیق صورت گیرد که در صورت بروز مشکل زودتر تشخیص داده شود.
کتامین افکار خودکشی را به سرعت کاهش میدهد
یافتههای مطالعه کارآزمایی بالینی تصادفی که در تاریخ ۵ دسامبر ۲۰۱۷ در American Journal of Psychaiatry منتشر شد حاكی از اين است كه اينفيوژن وریدی کتامین میتواند به سرعت افکار خودکشی را در بیمار مبتلا به افسردگی ماژور کاهش دهد و بهبودی بالینی تا ۶ هفته بعد باقی میماند.
در این مطالعه که بزرگترین مطالعه در این زمینه تاکنون است، ۸۰ بیمار افسرده با نمره افکار خودکشی ( SSI) بالاتر از ۴ به صورت داوطلبانه در بخش تحقیقاتی موسسه روانپزشکی نیویورک بستری شدند. ۴۰ بیمار کتامین هیدروکلراید وریدی با دوز نیم میلیگرم برای هر کیلو وزن
و۴۰ بیمار دیگر دو صدم میلیگرم برای هر کیلوگرم وزن میدازولام در ۱۰۰ سی سی نرمال سالین به صورت اینفیوژن دریافت کردند. علت انتخاب میدازولام برای مقایسه این است که داروی بیهوشی سایکواکتیو با نیمه عمری مشابه کتامین، و فاقد اثرات ضد افسردگی و ضد خودکشی است.
مشخصات پایه، از جمله نمره SSI در دو گروه مشابه بود. پاسخ درمانی به صورت ۵۰٪ کاهش در نمره SSI در نظر گرفته شد.
یافته ها: درصد بیمارانی که در روز اول پاسخ درمانی نشان دادند در گروه کتامین بیشتر بود ( p= 0.024).
محققين گزارش کردند که بهبودی در افکار خودکشی در طول دوره ۶ هفته مشاهده کنترل نشده باقی میماند. ممکن است بخشی از آن به علت ادامه داروهای سایکوتروپیک قبلی باشد که بعد از تجویز کتامین به اثر بهینه رسیدند.
در روز اول اینفیوژن کتامین در مقایسه با میدازولام، کاهش بیشتری در اختلال کلی خلق، افسردگی و خستگی حاصل شد. محققین معتقدند اثرات کتامین بر افسردگی و افکار خودکشی، حداقلیه صورت نسبی، مستقل هستند.
عوارض جانبی ( افزایش فشارخون و علائم تجزیهای) مشابه سایر مطالعات کتامین بود. این عوارض اکثرا خفیف تا متوسط و گذرا هستند و معمولا ظرف چند دقیقه تا چند ساعت بعد از اینفیوژن برطرف میشوند.
*دکتر ماندل، رئیس روانپزشکی بیمارستان هانتینگتون نیویورک، که شخصا در این مطالعه شرکت نداشته معتقد است که این میتواند یک مانور موقتی بسیار مفید و حافظ حیات در اورژانسها یا شرایط سرپایی باشد و زمان ارزشمندی بخرد تا درمان بتواند طی چند هفته به اثر بهینه برسد. این روش نه تنها در پیشگیری از خودکشی موثر است، بلکه میتواند هزینههای بستری را در بیمارانی که به صورت حاد در معرض خودکشیاند را کم کند. از این مطالعه مشخص نیست که بعد از ۶ هفته برای این بیماران چه اتفاقی خواهد افتاد. آیا افکار خودکشی برمیگردند، و اگر اینطور باشد آیا به تکرار درمان نیاز است؟ و برای چه مدت؟ اثرات طولانی مدت تکرار اینفیوژنها چیست؟ مطالعات بیشتری برای پاسخ به این سوالات لازم است.
داروهای آنتیکولینرژیک با خطر دمانس در بیماران اسکیزوفرنیا ارتباط دارند
اصطلاح “بار آنتی کولینرژیک (Anticholinergic burden )” به اثر تجمعی استفاده از چند دارو با محتویات آنتیکولینرژیک اشاره دارد.
داروهای متعددی که برای درمان اسکیزوفرنیا به کار میرود، شامل آنتیسایکوتیکها مثل کلوزاپین و الانزاپین، آنتیدپرسانتها، و تثبیت کنندههای خلق، فعالیت آنتیکولینرژیک مرکزی دارند. داروهای روانپزشکی تنها داروهایی نیستند که اثرات آنتیکولینرژیک دارند. آنالژزیکها، آنتیهیستامینها، ضدتهوعها، آنتیآریتمیکها، برونکودیلاتورها، و داروهای مورد استفاده برای بیاختیاری ادرار نیز این خواص را دارند. بسیاری ازبیماران مسنتر مبتلا به اسکیزوفرنیا مشکلات مدیکال دیگری نیز دارند و بنابراین ممکن است بار کولینرژیک بالا داشته باشند. همچنین آنها به عوارض جانبی آنتی کولینریک حساستر هستند.
طبق مطالعهای که به صورت آنلاین در ۲۸ نوامبر ۲۰۱۷ در Journal of Clinical Psychiatry منتشر شده، برای ارزیابی اثر بار آنتی کولینرژیک بر وضعیت شناختی، ۶۰ بیمار مبتلا به اسکیزوفرنیا با سن ۵۰ تا ۷۹ سال که نمره MMSE شان ۱۸ و بالاتر بود و افسردگی ماژور و اختلالات مصرف مواد و الکل نداشتند بررسی شدند.
در این مطالعه بار آنتیکولینرژیک داروهای مصرفی توسط هر بیمار محاسبه شد و ارتباط آن با عملکردهای شناختی اختصاصی بررسی گردید.
نتایج نشان داد که بیماران عملکرد ضعیفتری در حوزههای حافظه تاخیری، حافظه فوری، حافظه اپیزودیک، حافظه کارکردی-فضایی، و ساختار دیداری فضایی داشتند، ولی در آزمونهای توجه، عملکردهای اجرایی، زبان، یا زمان واکنش ضعف عملکرد نشان ندادند. برای مثال نمره کلی بار آنتیکولینرژیک ارتباط معناداری با حافظه کارکردی فضایی داشت ولی با یادگیری و زمان واکنش ارتباط معنادار نبود. همچنین ارتباط با ساختار دیداری -فضایی، حافظه فوری و حافظه تاخیری ارتباط معنادار بود.
در مورد زبان و توجه این اختلاف معنادارنبود. نویسندگان ذکر میکنند که نقائص حافظه اپیزودیک و توانایی دیداری -فضایی در اوایل سیر آلزایمر رخ میدهند در حالیکه مشکلات توجه و زبان تظاهرات تاخیری هستند.
مجموعا، این نتایج پیشنهاد میکنند که بار آنتیکولینرژیک بالا ممکن است منجر به نقائص شناختیای در بیمار اسکیزوفرنیا شوند که مشخصهی دمانس آلزایمر پره کلینیکال هستند
در مقایسه با جمعیت عمومی، بیماران دچار اسکیزوفرنیا دو برابر خطر بالاتری برای ابتلا به دمانس قبل از سن ۸۰ سالگی دارند. یافتههای جدید نشان میدهد که ممکن است بار آنتیکولینرژیک بالا مسوول بخشی از این افزایش خطر باشد. این نقائص ممکن است به اشتباه به پیشرفت بیماری اسکیزوفرنیا یا شروع دمانس منتسب شوند تا علت ثانویه قابل درمان، مثل بار آنتیکولینرژیک. بالینگران باید کاهش دوز این داروها و تغییر به داروهایی که کمتر آنتیکولینرژیک باشند را در نظر بگیرند.
محدودیت های احتمالی مطالعه
محققین اطلاعاتی درباره پذیرش درمان جمعآوری نکردند. همچنین دوزاژ دارو، تداخلات دارویی، یا وضعیت متابولیسم در نظر گرفته نشده است. با توجه به مقطعی بودن مطالعه و محدودیت حجم نمونه نمیتوان درباره رابطه علیتی بین بار آنتیکولینرژیک و نقص شناختی اظهار نظر کرد.
تایید فرم تزریقی ماهانهی بوپرهنورفین
سازمان غذا و داروی آمریکا (FDA) اولین و تنها فرمولاسیون قابل تزریق ماهیانهی بوپرنورفین را برای درمان بالغین مبتلا به اختلال مصرف متوسط تا شدید اوپیوئید تایید کرد.
بوپرنورفین ER (Sublocade ) به صورت زیر جلدی تجویز میشود و جمعیت هدف، افرادی هستند که درمان با بوپرنورفین ترانس موکوزال را شروع کردهاند و دوز آن تنظیم شده و حداقل ۷ روز دوز تنظیم شده را دریافت کردهاند.
دوز توصیه شدهی سابلوکید، ۳۰۰ میلیگرم ماهیانه در دو ماه ابتدایی و سپس دوز نگهدارنده ۱۰۰ میلیگرم در ماه است. افزایش دوز نگهدارنده تا ۳۰۰ میلیگرم در ماه را میتوان برای بیمارانی که فواید بیش از مضرات باشد، در نظر داشت.
این دارو فقط توسط مراقبین سلامت و در ترکیب با برنامه کامل درمانی شامل مشاوره و حمایت سایکوسوشیال تجویز میشود.
در كارآزمايیهای بالينی، اين دارو از نظر ايمنی مشابه بوپرنورفين ترنسموكوزال است به استثنای واكنشهای محل تزريق كه در ١٦/٥ درصد بيماران گزارش شده است. شايعترين واكنشهای ناخواسته (بيش از ٥ درصد بيماران) شامل يبوست، تهوع، استفراغ، سطح غير طبيعی آنزيمهای كبد، سردرد و خواب آلودگی است.
درباره اين دارو يك هشدار وجود دارد. در صورت تجويز وريدی خطر آسيب جدی و مرگ وجود دارد.
شركت سازنده پيشبينی میكند كه اين دارو در طول فصل اول ٢٠١٨ در ايالات متحده قابل دسترسی خواهد بود.
- منتشر شده در بیماری ها, داروها, گزارش و تحلیل